Niepożądane odczyny poszczepienne
Jakkolwiek autorzy opisu poniższego przypadku podkreślają, że "Ten przypadek pokazuje niezwykle rzadkie powikłanie szczepionki COVID-19. Korzyści z otrzymania preparatu przeciw COVID-19 przewyższają potencjalne ryzyko.", pozwala on nam po raz kolejny poddać refleksji bezpieczeństwo szczepień i zadać pytanie, czy można kogokolwiek zobowiązywać do przyjmowania preparatu, jeśli niesie to za sobą ryzyko ciężkich powikłań?
Ponadto pozostaje nieznany dalszy stan kondycji zdrowtnej osoby, u której wystąpiło poniższe powikłanie.
Czy każdy podobny przypadek zostanie zarejestrowany? Czy każdy będzie miał dostęp do natychmiastowego i kosztownego leczenia? Czy osoba obciążona innymi chorobami współistniejącymi wyjdzie z takiego pogorszenia stanu zdrowia bez konsekwencji?
Toxic Epidermal Necrolysis Post COVID-19 Vaccination - First Reported Case
Mohamad Bakir , Hanan Almeshal, Rifah Alturki, Sulaiman Obaid, Areej Almazroo
Opublikowano: 16 sierpień, 2021
DOI: 10.7759/cureus.17215
Cytowanie artykułu: Bakir M, Almeshal H, Alturki R, et al. (August 16, 2021) Toxic Epidermal Necrolysis Post COVID-19 Vaccination - First Reported Case. Cureus 13(8): e17215. doi:10.7759/cureus.17215
Streszczenie
Zespół Stevensa-Johnsona / toksyczne martwicze oddzielanie się naskórka (SJS/TEN) to spektrum ostrych reakcji nadwrażliwości typu opóźnionego, które dotyczą skóry i błon śluzowych. Przyczyną tych zaburzeń są leki, a także infekcje i w bardzo rzadkich przypadkach szczepienia. Przedstawiamy przypadek TEN u 49-letniej kobiety bez wcześniejszej historii choroby. Zaburzenie rozwinęło się tydzień po otrzymaniu pierwszej dawki szczepionki COVID-19 bez innych możliwych do zidentyfikowania przyczyn. Pacjentka otrzymała dwie dawki inhibitora czynnika martwicy nowotworu alfa (etanercept) i po dwóch dniach od dawki początkowej przestały rozwijać się nowe zmiany; całkowite wygojenie nastąpiło po 22 dniach i u naszego pacjenta nie zaobserwowano żadnych skutków ubocznych. Ten przypadek pokazuje niezwykle rzadkie powikłanie szczepionki COVID-19. Korzyści z otrzymania preparatu przeciw COVID-19 przewyższają potencjalne ryzyko.
Prezentacja przypadku
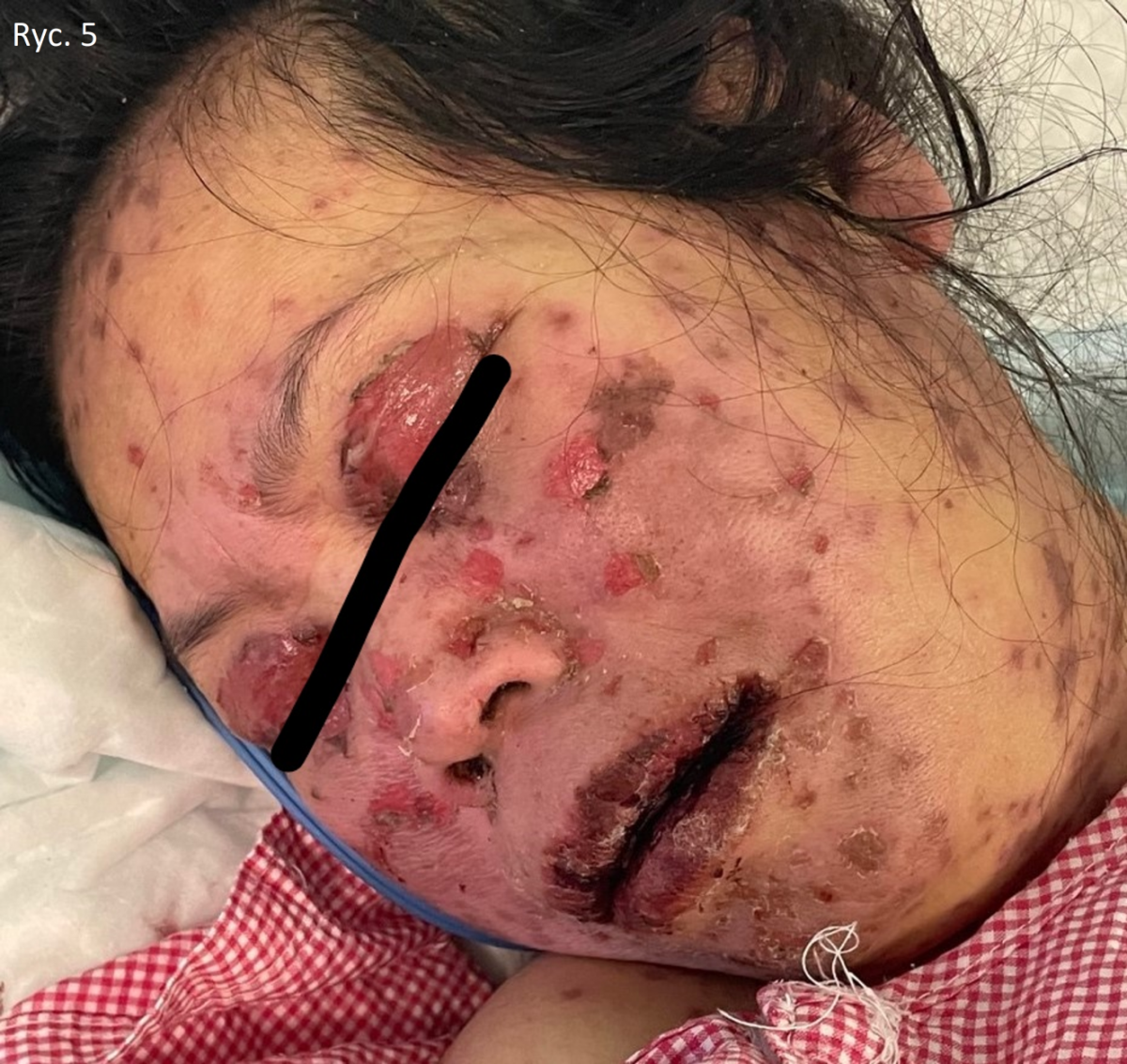
49-letnia kobieta bez wcześniejszej historii medycznej zgłosiła się na izbę przyjęć z historią gorączki i wykwitów skórnych. Otrzymała szczepionkę COVID-19 Pfizer (BNT162b1) w dawce 0,3 ml podawaną domięśniowo na tydzień przed wystąpieniem u niej objawów. U pacjentki pojawiła się gorączka, zmęczenie i bóle głowy, a następnie zmiany skórne obejmujące tułów, które zaczęły rozprzestrzeniać się na twarz i kończyny górne z owrzodzeniem jamy ustnej. Pacjentka przebywała w POZ, otrzymała paracetamol i nie zauważyła poprawy. Pacjentka nie miała historii przyjmowania nowych leków ani zabiegów kosmetycznych w ciągu ostatnich dwóch miesięcy przed pojawieniem się zmian skórnych. Podczas badania pacjentka była stabilna, niespokojna i odczuwała silny ból. Miała liczne purpurowe i ciemnoczerwone plamki obejmujące klatkę piersiową (ryc. 1), brzuch (ryc. 2), kończyny górne (ryc. 3), twarz, narządy płciowe i górną część ud z obszarami wykazującymi zlewanie się zmian z wiotkimi pęcherzami i obszarami odwarstwienia naskórka z pozytywnym objawem Nikolskiego. Jej stan obejmował błonę śluzową, w której wystąpiły rozległe owrzodzenia jamy ustnej i krwotoczne strupy na wargach (ryc. 4), a także obustronne przekrwienie spojówek wraz z nadżerkami powiek górnych (ryc. 5) oraz zmiany na błonach śluzowych narządów płciowych. Powierzchnię ciała (BSA) objętą zmianami szacuje się na ponad 30%. Badania laboratoryjne wykazały niski poziom białych krwinek (3,87 × 109/l) i podwyższony poziom enzymów wątrobowych (aminotransferaza asparaginianowa [AST] 178 j./l, aminotransferaza alaninowa [ALT] 90 j./l). Prześwietlenie klatki piersiowej było w normie, a serologia była negatywna w kierunku wirusowego zapalenia wątroby typu B, C i HIV. Skala ciężkości choroby dla toksycznej martwicy naskórka (SCORTEN) wynosiła dwa w dniu przyjęcia, ponieważ pacjentka miała ponad 40 lat, a poziom wodorowęglanów w surowicy był niższy niż <20 mmol/l.
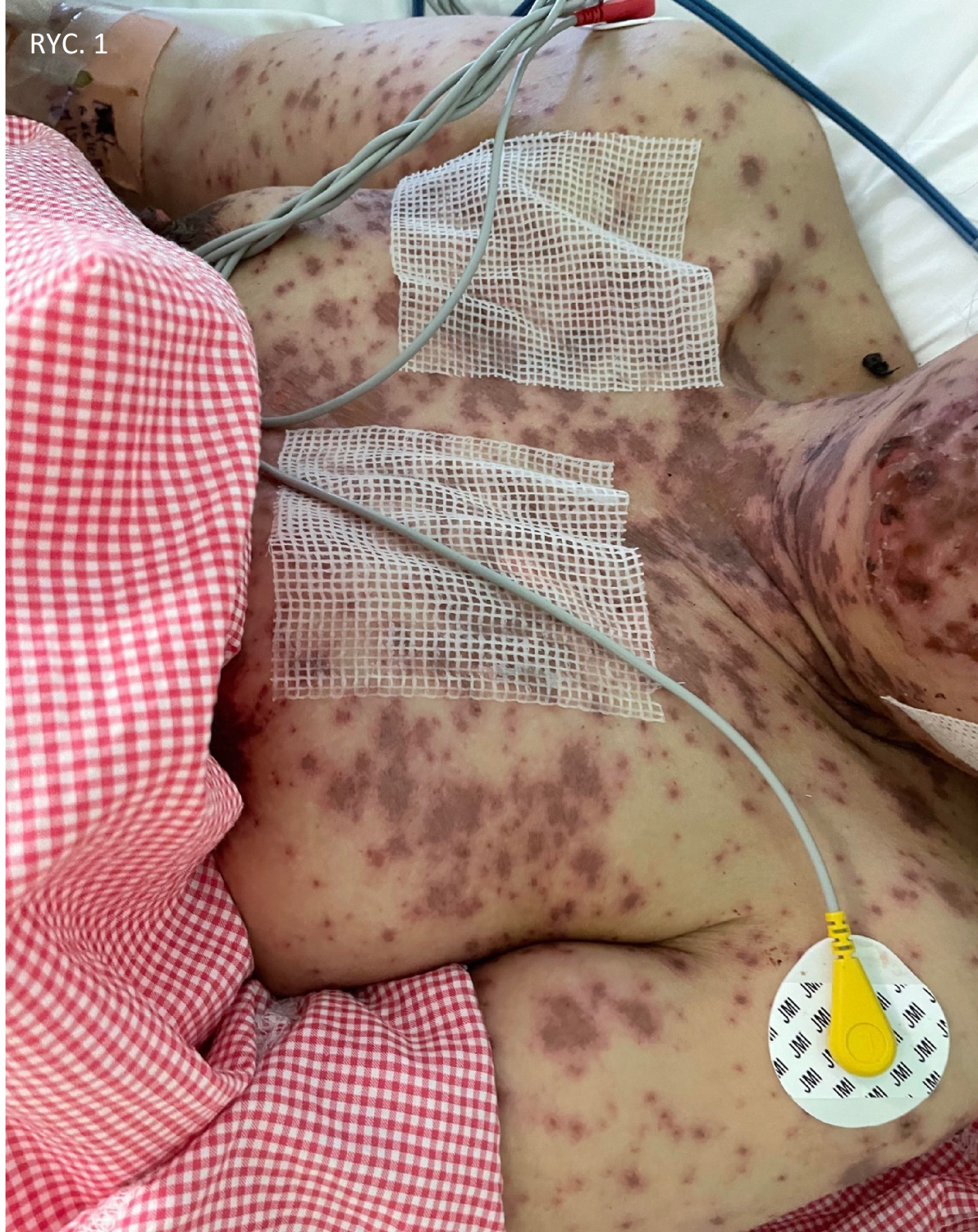
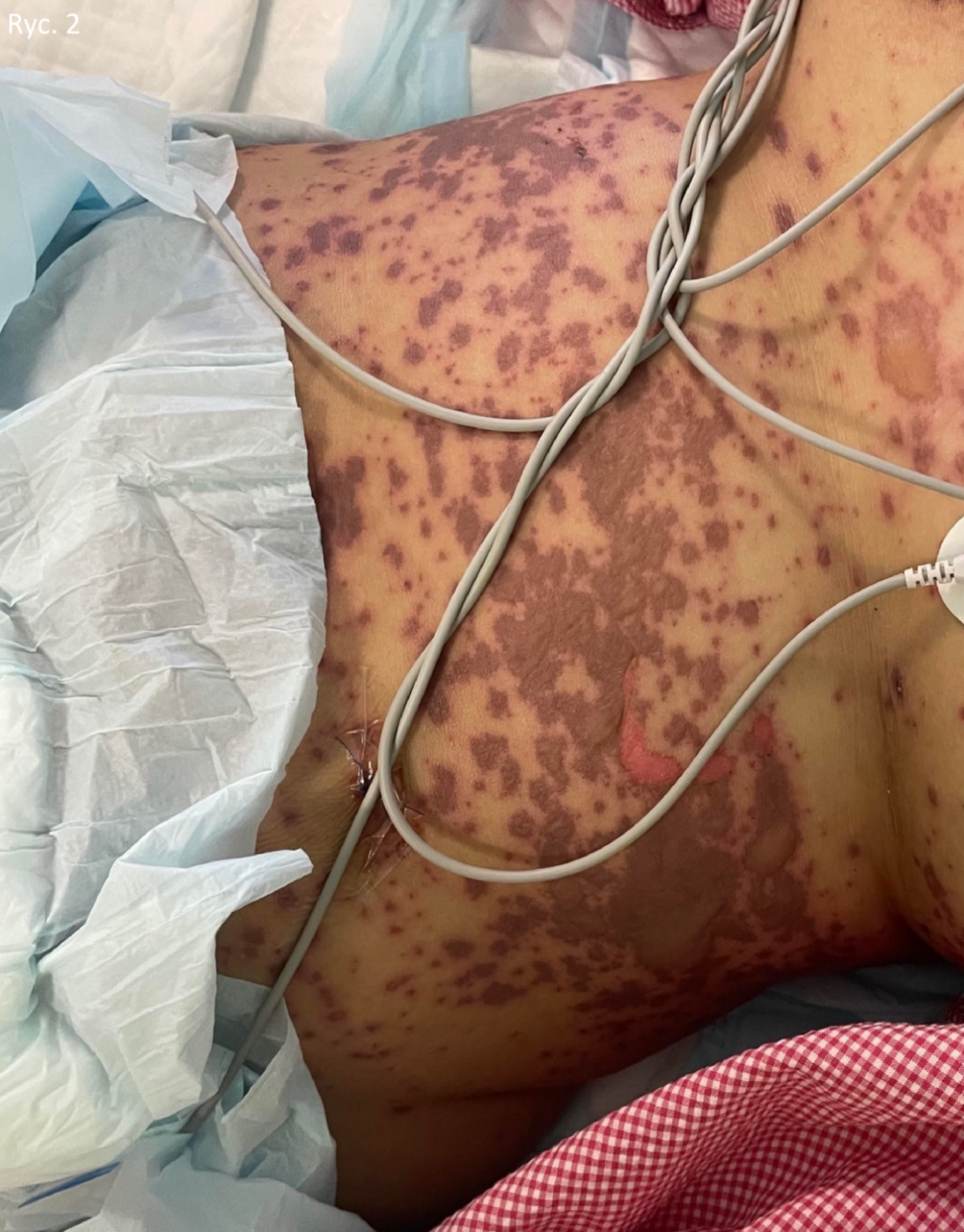
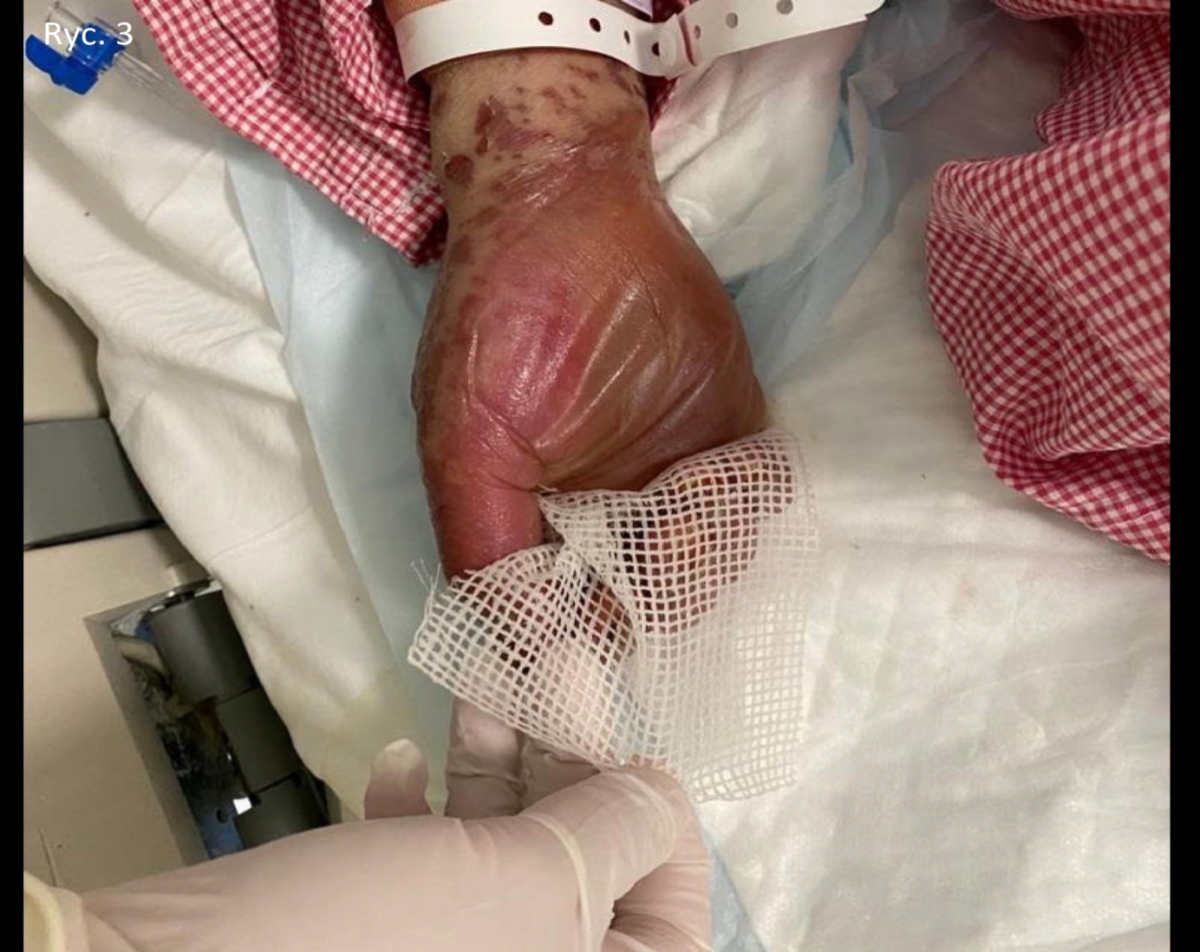
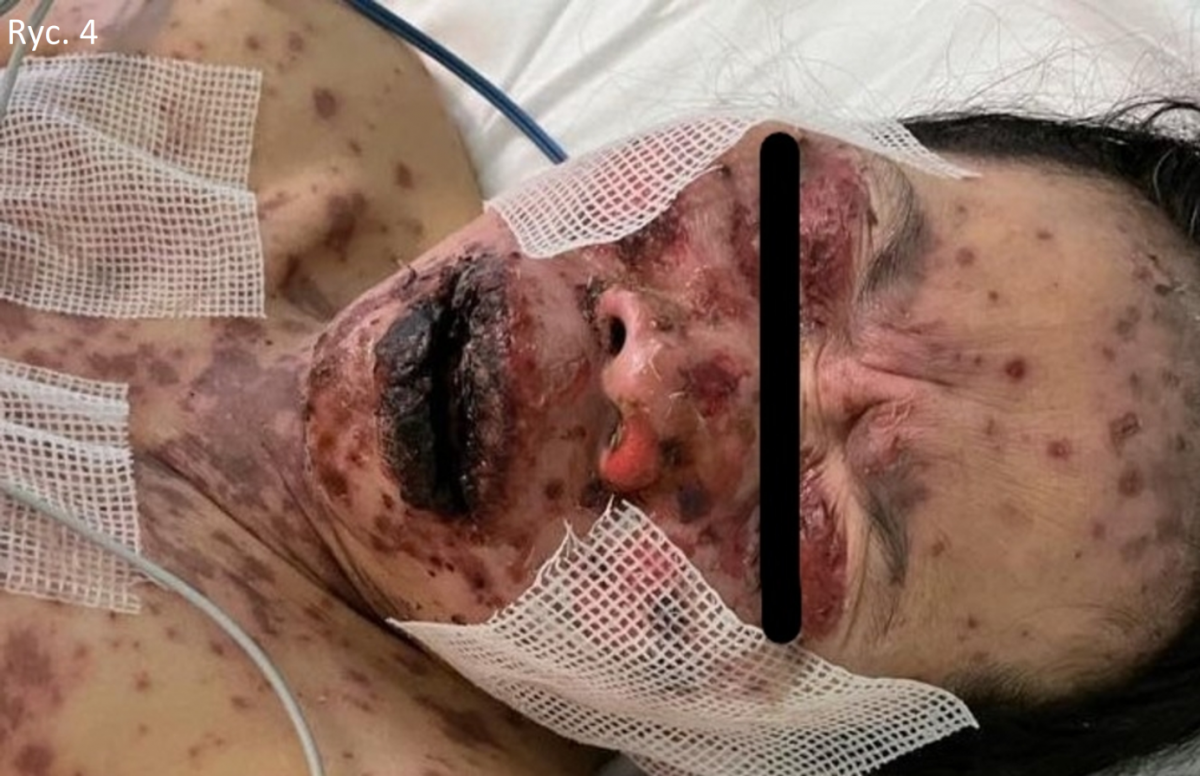
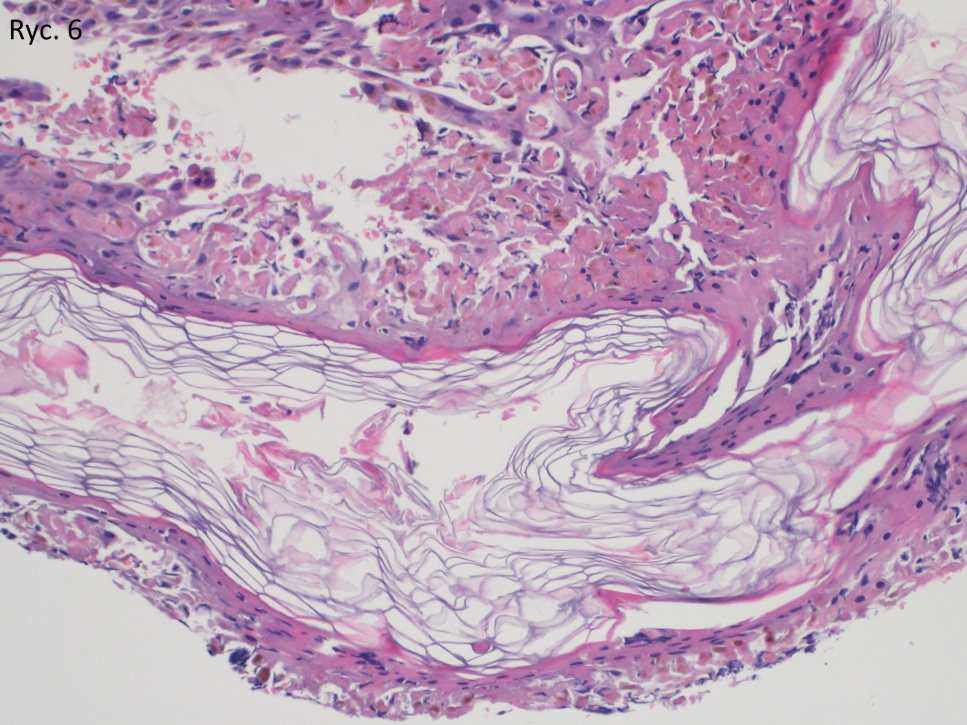
Badanie histopatologiczne zmiany wykazało martwicę naskórka pełnej grubości wraz z separacją skórno-naskórkową i martwiczymi keratynocytami (ryc. 6).
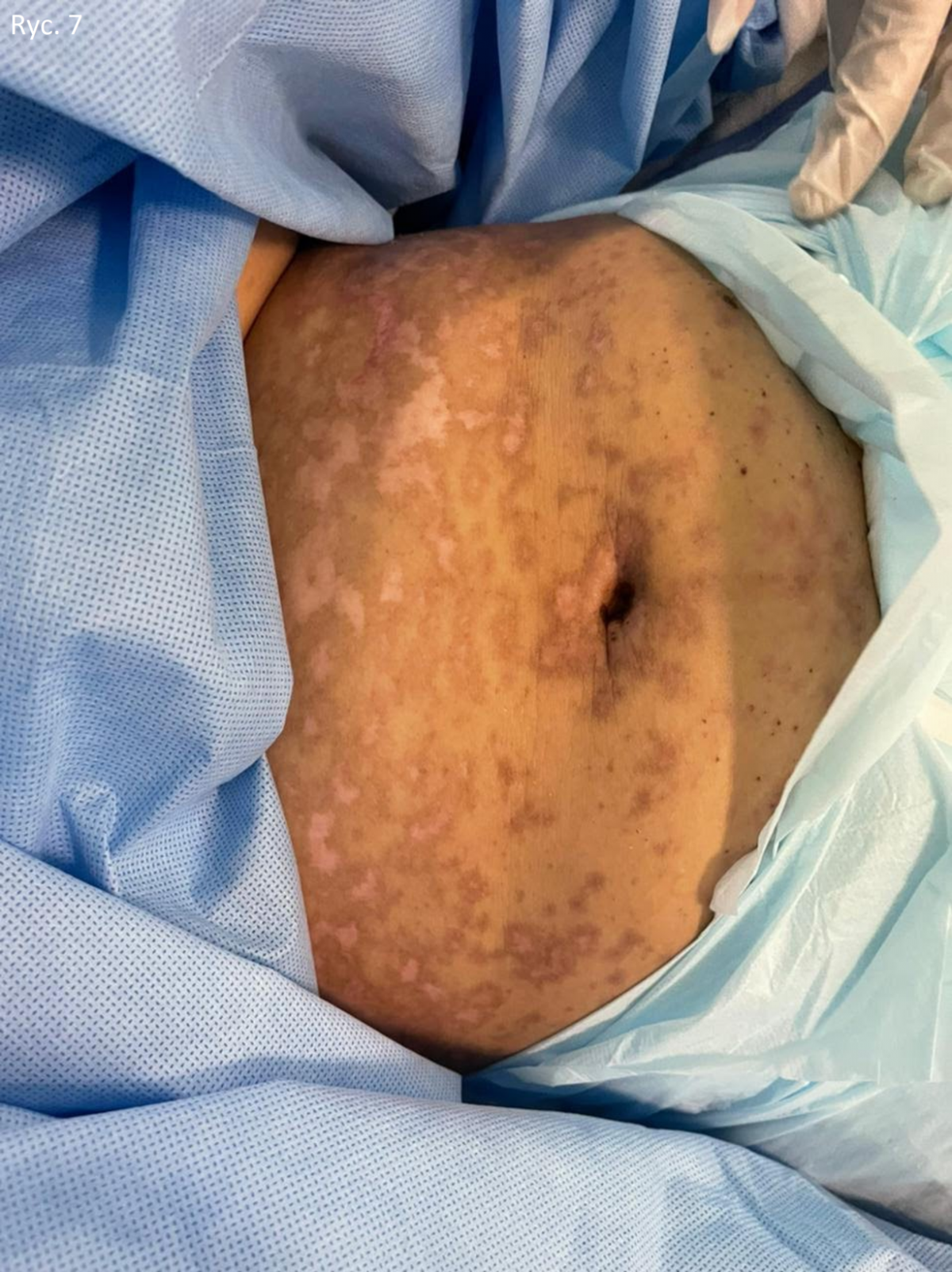
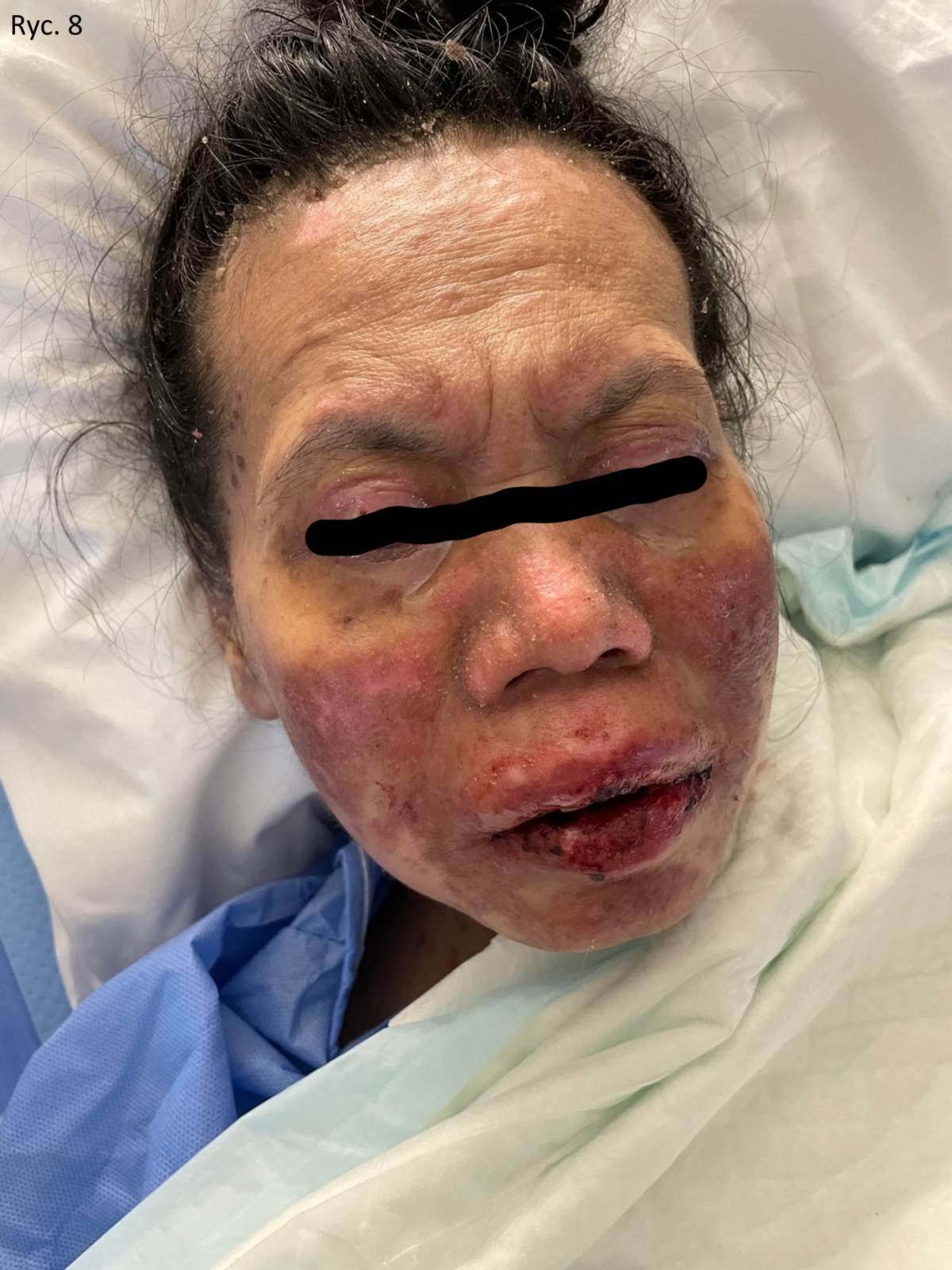
Pacjentka została przyjęta do szpitala na oddział HDU i traktowana w sposób aseptyczny; Rozpoczęto dożylną infuzję płynów i składników odżywczych. Zespoły okulistyczne, położnicze, ginekologiczne i urologiczne były zaangażowane w leczenie przypadku, ponieważ jej choroba dotyczyła oczu i potrzebowała miejscowych antybiotyków i miejscowych środków nawilżających. Ponadto miała nadżerki, które obejmowały jej narządy płciowe, więc zastosowano miejscowo opatrunki z gazy i wazeliny, a zespoły położniczo-ginekologiczne i urologiczne obserwowały ją, aby zapobiec przyszłym powikłaniom. Pacjentce podano podskórnie dwie dawki etanerceptu 50 mg/ml, pierwszą w dniu przyjęcia, a drugą po dwóch dniach od przyjęcia. Po dwóch dniach od podania pierwszej dawki pacjentka przestała rozwijać nowe zmiany, a całkowite wygojenie zaobserwowano po 22 dniach (ryc. 7, 8). U naszej pacjentki nie odnotowano żadnych skutków ubocznych.
Dyskusja
SJS/TEN to grupa rzadkich, ciężkich i potencjalnie śmiertelnych reakcji nadwrażliwości typu IV. Leki są zdecydowanie najczęstszą przyczyną tych schorzeń. Jednak SJS/TEN mogą być w bardzo rzadkich przypadkach spowodowane szczepieniem [5]. Zaczyna się od objawów grypopodobnych, po których następuje bolesna wysypka, która się rozprzestrzenia i pęcherzuje. Zmiany w TEN składają się ze zmian o wyglądzie kropek i purpurowych plam z martwicą naskórka na pełnej grubości, wraz z zajęciem błony śluzowej. TEN jest uważany za nagły przypadek medyczny, który wymaga pilnej interwencji medycznej, w którym czynnik sprawczy, jeśli jest obecny, powinien zostać natychmiast odstawiony. Najbardziej zaangażowane miejsca w SJS/TEN to twarz, dłonie, podeszwy i przedmostkowa część tułowia. Ponadto często zaangażowana jest błona śluzowa narządów płciowych, oczu i policzków [8]. W SJS zajęte jest mniej niż 10% powierzchni ciała, podczas gdy w TEN ponad 30% powierzchni ciała. Jeśli zajęcie skóry wynosi od 10% do 30%, uważa się to za nakładanie się SJS-TEN. Uważa się, że patofizjologia rozwoju SJS/TEN to swoiste dla leku limfocyty CD8+, w których te cytotoksyczne limfocyty T uwalniają granulizynę, granzym B i perforynę - enzymy te prowadzą do tworzenia porów i aktywacji kaskady śmierci w dotkniętych komórkach. Ponadto, czynnik martwicy nowotworu (TNF)-alfa i interferon-gamma są wydzielane w znacznych ilościach przez aktywowane komórki T, co prowadzi do nadekspresji ligandów Fas i śmierci keratynocytów za pośrednictwem Fas [9] (Figura 9).
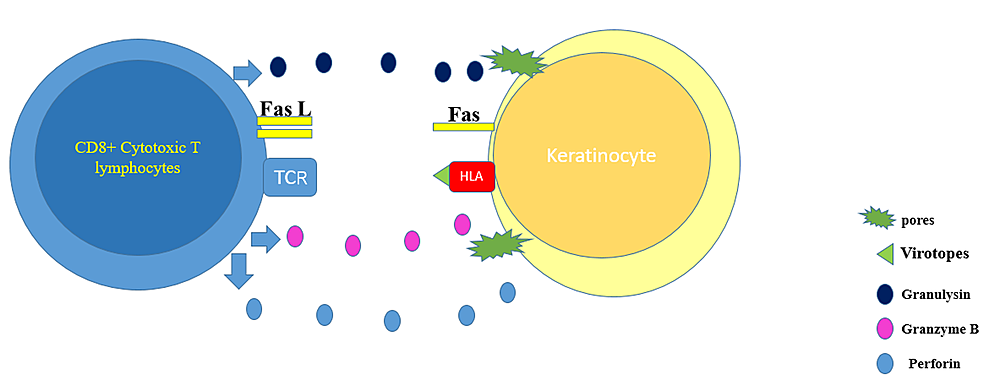
Szczepionka COVID-19 składa się z dwóch składników. Postawiono hipotezę, że antygen wirotopowy, który ulega ekspresji na powierzchni keratynocytów, może prowadzić do aktywacji cytotoksycznych limfocytów T i śmierci komórek naskórka [10, 11]. SJS/TEN to diagnoza kliniczna i histopatologiczna. W badaniu histopatologicznym stwierdza się martwicę keratynocytów i skórnego nacieku limfocytarnego z ujemnym docelowym testem immunofluorescencyjnym. Pacjenci z TEN wymagają leczenia wspomagającego, takiego jak odstawienie czynnika(ów) wywołującego(ych), przyjęcie na oddział intensywnej terapii lub oddział oparzeń, uzupełnienie płynów i elektrolitów, karmienie tubą nosowo-żołądkową lub całkowite żywienie pozajelitowe wraz z kontrolą bólu i temperatury. Sepsa i niewydolność narządów to najpoważniejsze powikłania TEN. Wykazano, że poziomy TNF-alfa są podwyższone w próbkach z biopsji skóry, płynie pęcherzowym i surowicy pacjentów z TEN, co zachęca do stosowania terapii biologicznej wykorzystującej działanie anty-TNF-alfa [12, 13]. W jednym z badań pojedyncza dawka etanerceptu (Enbrel, Immunex Corporation, Seattle, USA) 50 mg/ml podskórnie wydawała się modyfikować przebieg choroby, w której znaczne zmniejszenie obrzęku i zatrzymanie rozwoju choroby zauważono już po 24 godzinach [14]. W ostatnich latach stosowano antagonistów TNF-alfa, a w większości przypadków zaobserwowano znaczną poprawę, w której tworzenie zmian ustało w ciągu dwóch dni, a całkowite ustąpienie nastąpiło w ciągu 20 dni. Również u pacjentów z SJS/TEN leczonych etanerceptem nie udokumentowano żadnych poważnych działań niepożądanych. Ponadto, w porównaniu do osób, którym podawano kortykosteroidy, obserwowano niższy odsetek krwotoków z przewodu pokarmowego oraz obniżony poziom ekspresji granulizyny i TNF-alfa [15]. Plazmafereza, dożylna immunoglobulina (IVIG) i być może najbardziej obiecujące inhibitory TNF, takie jak etanercept, są możliwościami leczenia TEN wywołanego szczepionką [14]. Jednak nadal kontrowersyjne jest stosowanie IVIG i dużych dawek kortykosteroidów ogólnoustrojowych [16]. Uważa się, że plazmafereza działa u pacjentów z TEN w oparciu o założenie usunięcia leku, metabolitu leku lub mediatora cytotoksycznego z krążenia. Jednak jedno szwedzkie badanie nie wykazało korzyści z plazmaferezy u ośmiu pacjentów w porównaniu z pacjentami w innych badaniach, którzy otrzymali równoważną opiekę wspomagającą, ale nie plazmaferezę [17]. Na tym etapie nie ma wystarczających danych uzasadniających zastosowanie plazmaferezy w stosunku do innych metod wspomagających [18]. W randomizowanym kontrolowanym badaniu porównującym skuteczność etanerceptu i kortykosteroidów u pacjentów z SJS/TEN stwierdzono, że etanercept wspomaga gojenie skóry i błony śluzowej jamy ustnej oraz ułatwia odbudowę nabłonka [15]. Według naszej wiedzy jest to pierwszy odnotowany przypadek TEN po szczepieniu preparatem Pfizer przeciw COVID-19. Były dwa przypadki SJS po szczepieniu COVID-19, w pierwszym przypadku nie wymieniono nazwy ani dawki szczepionki, którą otrzymał ich pacjent [11]. Jednak w drugim przypadku wspomnieli, że ich pacjent rozwinął SJS po otrzymaniu drugiej dawki szczepionki Pfizer COVID-19 [19]. Nasz pacjent całkowicie wyzdrowiał po otrzymaniu dwóch dawek etanerceptu.
Wnioski
Ten przykład podkreśla niezwykle rzadkie powikłanie poszczepienne. Ale korzyści znacznie przewyższają ryzyko w obecnych okolicznościach, dlatego wśród społeczności nie powinno być wahania w kwestii szczepień. Dlatego zgłaszając ten przypadek, podkreślamy rzadkość występowania tego efektu ubocznego, a biorąc pod uwagę okoliczności, nie powinno to wpływać na decyzję o przyjęciu szczepionki ani pogłębiać istniejących tam niejasności. W naszym przypadku wyjaśniliśmy patofizjologię rozwoju toksycznej nekrolizy naskórka w następstwie szczepienia oraz podkreśliliśmy skuteczność eternaceptu jako bezpiecznego i szybkiego leczenia tego schorzenia.
Piśmiennictwo
- Schwartz RA, McDonough PH, Lee BW: Toxic epidermal necrolysis: Part I. Introduction, history, classification, clinical features, systemic manifestations, etiology, and immunopathogenesis. J Am Acad Dermatol. 2013, 69:173.e1-13; quiz 185-6. 10.1016/j.jaad.2013.05.003
- Schwartz RA, McDonough PH, Lee BW: Toxic epidermal necrolysis: Part II. Prognosis, sequelae, diagnosis, differential diagnosis, prevention, and treatment. J Am Acad Dermatol. 2013, 69:187.e1-16; quiz 203-4. 10.1016/j.jaad.2013.05.002
- Mockenhaupt M: Epidemiology of cutaneous adverse drug reactions. Chem Immunol Allergy. 2012, 97:1-17. 10.1159/000335612
- Rosenblatt AE, Stein SL: Cutaneous reactions to vaccinations. Clin Dermatol. 2015, 33:327-32. 10.1016/j.clindermatol.2014.12.009
- Ball R, Ball LK, Wise RP, Braun MM, Beeler JA, Salive ME: Stevens-Johnson syndrome and toxic epidermal necrolysis after vaccination: reports to the vaccine adverse event reporting system. Pediatr Infect Dis J. 2001, 20:219-23. 10.1097/00006454-200102000-00022
- Dobrosavljevic D, Milinkovic MV, Nikolic MM: Toxic epidermal necrolysis following morbilli-parotitis-rubella vaccination. J Eur Acad Dermatol Venereol. 1999, 13:59-61.
- Harr T, French LE: Stevens-Johnson syndrome and toxic epidermal necrolysis. Chem Immunol Allergy. 2012, 97:149-66. 10.1159/000335627
- Grazina I, Mannocci A, Meggiolaro A, La Torre G: Is there an association between Stevens-Johnson Syndrome and vaccination? A systematic review. Ann Ig. 2020, 32:81-96. 10.7416/ai.2020.2333
- Oakley AM, Krishnamurthy K: Stevens Johnson Syndrome. StatPearls [Internet]. StatPearls Publishing (ed): Treasure Island, 2021; 2021 Jan-.
- Stone CA Jr, Rukasin CR, Beachkofsky TM, Phillips EJ: Immune-mediated adverse reactions to vaccines. Br J Clin Pharmacol. 2019, 85:2694-706. 10.1111/bcp.14112
- Dash S, Sirka CS, Mishra S, Viswan P: Covid-19 vaccine induced Steven-Johnson syndrome: a case report. Clin Exp Dermatol. 2021, 10.1111/ced.14784
- Paquet P, Paquet F, Al Saleh W, Reper P, Vanderkelen A, Piérard GE: Immunoregulatory effector cells in drug-induced toxic epidermal necrolysis. Am J Dermatopathol. 2000, 22:413-7. 10.1097/00000372-200010000-00005
- Posadas SJ, Padial A, Torres MJ, et al.: Delayed reactions to drugs show levels of perforin, granzyme B, and Fas-L to be related to disease severity. J Allergy Clin Immunol. 2002, 109:155-61. 10.1067/mai.2002.120563
- Chahal D, Aleshin M, Turegano M, Chiu M, Worswick S: Vaccine-induced toxic epidermal necrolysis: a case and systematic review. Dermatol Online J. 2018241, 13030-7. 10.5070/D3241037941
- Wang CW, Yang LY, Chen CB, et al.: Randomized, controlled trial of TNF-α antagonist in CTL-mediated severe cutaneous adverse reactions. J Clin Invest. 2018, 128:985-96. 10.1172/JCI93349
- St John J, Ratushny V, Liu KJ, et al.: Successful use of cyclosporin a for Stevens-Johnson syndrome and toxic epidermal necrolysis in three children. Pediatr Dermatol. 2017, 34:540-6. 10.1111/pde.13236
- Furubacke A, Berlin G, Anderson C, Sjöberg F: Lack of significant treatment effect of plasma exchange in the treatment of drug-induced toxic epidermal necrolysis?. Intensive Care Med. 1999, 25:1307-10. 10.1007/s001340051063
- Fernando SL: The management of toxic epidermal necrolysis. Australas J Dermatol. 2012, 53:165-71. 10.1111/j.1440-0960.2011.00862.x
- Elboraey MO, Essa EE: Stevens-Johnson syndrome post second dose of Pfizer COVID-19 vaccine: a case report. Oral Surg Oral Med Oral Pathol Oral Radiol. 2021, 10.1016/j.oooo.2021.06.019
Zdjęcia/grafiki - źródło: https://www.cureus.com/articles/68051-toxic-epidermal-necrolysis-post-covid-19-vaccination---first-reported-case
Opracował: lek.stom. Remigiusz Cop








