Niepożądane odczyny poszczepienne
"Szybka progresja chłoniaka angioimmunoblastycznego z komórek T po podaniu dawki przypominającej szczepionki BNT162b2 mRNA. Opis przypadku"
"Wkrótce po rozpoczęciu kampanii szczepień przeciwko SARS-CoV-2 okazało się, że wstrzyknięcie szczepionek mRNA może wywołać obrzęk węzłów chłonnych drenujących miejsce wstrzyknięcia. Chociaż uważana za łagodną, ta reakcja na szczepionkę czasami komplikowała interpretację obrazowania 18F-FDG PET/CT pod kątem podejrzenia procesu nowotworowego dotyczącego węzłów chłonnych (3). (...)"
"Rapid Progression of Angioimmunoblastic T Cell Lymphoma Following BNT162b2 mRNA Vaccine Booster Shot: A Case Report"
https://pubmed.ncbi.nlm.nih.gov/34901098/
Opublikowano online 25 listopada 2021 roku: 10.3389/fmed.2021.798095
Autorzy: Serge Goldman,1 Dominique Bron,2 Thomas Tousseyn,3 Irina Vierasu,1 Laurent Dewispelaere,4 Pierre Heimann,4 Elie Cogan5 i Michel Goldman6, *
Streszczenie
Ponieważ szczepionki mRNA modyfikowane nukleozydami silnie aktywują pomocnicze komórki pęcherzykowe T, ważne jest zbadanie możliwego wpływu zatwierdzonych (obecnie tymczasowo) szczepionek mRNA SARS-CoV-2 na nowotwory wpływające na ten typ komórek. W niniejszym dokumencie opisujemy i omawiamy nieoczekiwaną szybką progresję zmian chłoniakowych po podaniu przypominającej dawki szczepionki mRNA BNT162b2 u mężczyzny, u którego niedawno zdiagnozowano chłoniaka angioimmunoblastycznego (AITL).
Słowa kluczowe: szczepionka mRNA, limfocyty T, chłoniak, COVID-19, angioimmunoblastyczny, pęcherzykowy.
Wstęp
Działanie modyfikowanych nukleozydami szczepionek mRNA SARS-CoV-2 zostało powiązana z ich zdolnością do indukowania silnej stymulacji komórek pomocniczych T (TFH), co skutkuje utrzymującymi się odpowiedziami komórek B ośrodka namnażania (1, 2). Klinicznie może to przekładać się na reaktywną limfoadenopatię, która czasami może skłaniać do postawienia diagnozy różnicowej z zaburzeniem limfoproliferacyjnym (3, 4). Jednocześnie potencjalny wpływ szczepienia SARS-CoV-2 mRNA na wykryty wcześniej chłoniak z obwodowych komórek T wymaga dalszych badań i ustalenia.
Opis przypadku
Sześćdziesięciosześcioletni mężczyzna bez znaczącej historii medycznej poza nadciśnieniem, hipercholesterolemią i cukrzycą typu 2 zgłosił się 1 września 2021 roku z limfadenopatiami szyjnymi, które ujawniły się niedawno podczas zespołu grypopodobnego. Dwie dawki szczepionki BNT162b2 mRNA podano odpowiednio 5 i 6 miesięcy wcześniej w lewe ramię. Poza umiarkowaną astenią pacjent nie zgłosił żadnych istotnych objawów. Badanie krwi wykazało łagodny zespół zapalny, bez anemii i zmian w krwinkach białych; Immunofenotypowanie limfocytów nie było znaczące. Elektroforeza białek i poziomy immunoglobulin były prawidłowe, a test Coombsa był ujemny.
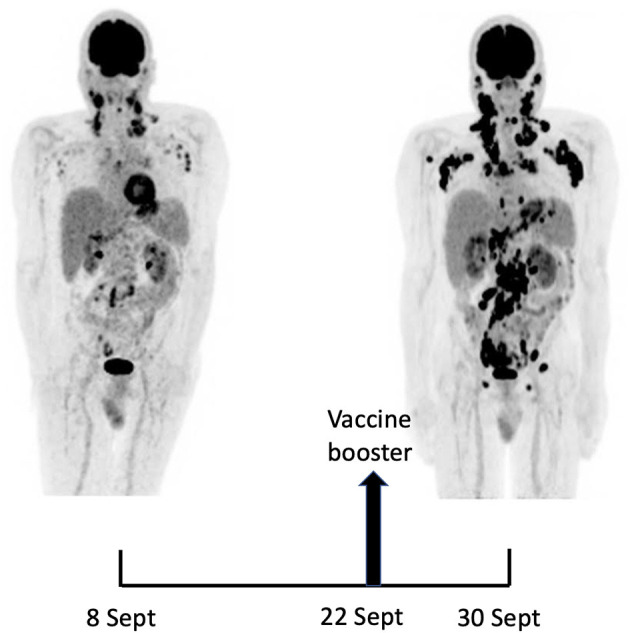
Badanie PET/CT 18F-FDG ujawniło liczne, rozległe hipermetaboliczne limfadenopatie powyżej i poniżej przepony, a także kilka pozawęzłowych zmian hipermetabolicznych (ryc. 1, lewy panel). Biorąc pod uwagę wstępne rozpoznanie chłoniaka w IV stopniu zaawansowania, wykonano biopsję lewego węzła chłonnego szyjnego. Badanie patologiczne ujawniło resztkowe zanikowe ośrodki namnażania otoczone rozszerzonym obszarem przykorowym złożonym z nietypowego nacieku limfocytów T o wyraźnej morfologii komórek, wykazujących ekspresję markerów komórek TFH (CD3, CD4, PD1, ICOS, BCL6, CXCL13) oraz utratę CD7. Obszar przykorowy zawierał zwiększoną liczbę wysoko śródbłonkowych żyłek, wspartych zwiększoną liczbą pęcherzykowych sieci komórek dendrytycznych, z pewnymi ogniskami proliferacji immunoblastycznej limfocytów B EBV+ w tle (ryc. 2). Cechy te wysoce sugerowały diagnozę angioimmunoblastycznego chłoniaka z komórek T (AITL), wzór 2. Sekwencjonowanie nowej generacji (NGS) przeprowadzone na próbce z biopsji zidentyfikowało mutację RHOA G17V charakterystyczną dla AITL (5) wraz z mutacjami DNMT3A, IDH2 i TET2. Rearanżacja genu TCR-gamma potwierdziła proliferację klonalnych komórek T. W sumie wyniki te jednoznacznie postawiły diagnozę chłoniaka angioimmunoblastycznego (AITL). Biopsja szpiku kostnego nie wykazała ani nieprawidłowości morfologicznych, ani fenotypowych, ale NGS ujawniło mutacje DMNT3A i TET2 w komórkach szpiku kostnego z częstością alleli odpowiednio 41% i 36%.
Zdjęcie 1
Zdjęcie 2
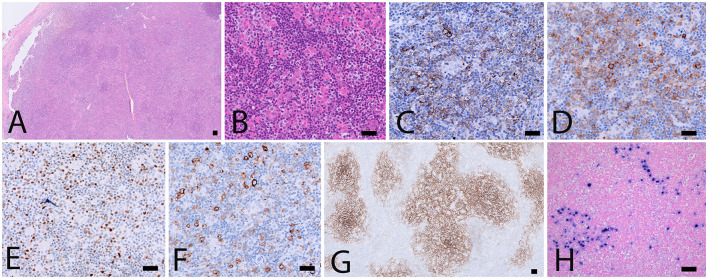
Próbka z biopsji. (A, B) Barwienia H&E wykazujące zaburzenia architektoniczne spowodowane populacją limfoidalną średniej wielkości z wyraźną morfologią komórek. (C-F) Barwienia immunohistochemiczne określające pochodzenie TFH nieprawidłowej populacji komórek: CD3+, CD4+, CD10+ (nie pokazano), ICOS+ (C), PD1 (D), BCL6 (E) i ekspresja CD30 (F). Barwienie CD21 (G) pokazuje rozszerzoną sieć pęcherzykowych komórek dendrytycznych. (H) Immunoblasty EBV+ o średniej wielkości przez hybrydyzację EBER in situ. Skala: 100 μm.
Czternaście dni po PET/CT pacjentowi podano dawkę przypominającą szczepionki BNT162b2 mRNA w prawy mięsień ramienny, w ramach przygotowań do pierwszego cyklu chemioterapii. W ciągu kilku dni po podaniu dawki przypominającej, pacjent zgłosił zauważalny obrzęk węzłów chłonnych szyjnych po prawej stronie. W celu uzyskania linii bazowej bliskiej początku terapii, drugi 18F-FDG PET/CT wykonano 8 dni po podaniu dawki przypominającej, tj. 22 dni po pierwszym.
Ujawniono wyraźny wzrost liczby, wielkości i aktywności metabolicznej istniejących wcześniej limfadenopatii na poziomie nad- i podprzeponowym. Ponadto od czasu pierwszego badania rozwinęły się nowe hipermetaboliczne limfadenopatie i nowe hipermetaboliczne miejsca w kilku różnych lokalizacjach (ryc. 1, prawy panel). Do oceny zmian czynności węzłów chłonnych wykorzystano wskaźnik całkowitej glikolizy zmian (TLG) (6). W porównaniu z testem początkowym nastąpił wyraźny 5,3-krotny wzrost TLG całego ciała, przy czym wzrost w teście po podaniu dawki przypominającej był dwukrotnie wyższy w prawej okolicy pachowej niż w lewej. Jednocześnie odnotowano niewielki wzrost poziomu ferrytyny we krwi, białka C-reaktywnego i LDH.
Podawanie metyloprednizolonu rozpoczęto natychmiast po drugim badaniu PET/TK, a następnie zastosowano pierwszy cykl brentuksymab vendotin w połączeniu z cyklofosfamidem, doksorubicyną (BV-CHP) zgodnie z niedawno opublikowanym protokołem (7). W chwili powstania tego doniesienia, 2 tygodnie po rozpoczęciu leczenia, badanie kliniczne wskazuje na znaczne zmniejszenie obrzęku węzłów chłonnych szyjnych i pachowych oraz poprawę ogólnego stanu sprawności pacjenta. Co ważne, porównanie poziomów przeciwciał anty-SARS-CoV-2 bezpośrednio przed i 21 dni po podaniu dawki przypominającej nie wykazało znaczącej zmiany w wytwarzaniu przeciwciał dla białka szczytowego (kolca) (171 vs 147 jednostek przeciwciała wiążącego/ml).
Dyskusja
Wkrótce po rozpoczęciu kampanii szczepień przeciwko SARS-CoV-2 okazało się, że wstrzyknięcie szczepionek mRNA może wywołać obrzęk węzłów chłonnych drenujących miejsce wstrzyknięcia. Chociaż uważana za łagodną, ta reakcja na szczepionkę czasami komplikowała interpretację obrazowania 18F-FDG PET/CT pod kątem podejrzenia procesu nowotworowego dotyczącego węzłów chłonnych (3). Po wykonaniu u pacjenta biopsji węzłów chłonnych w celu wykluczenia procesu nowotworowego, obraz patologiczny wykazywał reaktywne zmiany łagodne z widocznymi ośrodkami rozmnażania (3, 8). Diagnostyka różnicowa z chłoniakiem była czasami komplikowana przez rozwój hipermetabolicznych miejsc w odległości od miejsca wstrzyknięcia, w tym przeciwległych węzłów chłonnych lub śledziony (9, 10). U pacjenta z chłoniakiem z komórek płaszcza badanie PET/CT sugerowało nawrót, ale ostatecznie zostało wykluczone (11).
Opublikowane badania dotyczące hipermetabolicznej limfadenopatii po szczepieniu SARS-CoV-2 zostały niedawno poddane przeglądowi i poddane metaanalizie (8, 12). Większość obserwacji odnotowano po wstrzyknięciu zatwierdzonych szczepionek mRNA modyfikowanych nukleozydami, a mianowicie BNT162b2 (Pfizer-BioNTech) lub mRNA-173 (Moderna) (8). Niemniej jednak hipermetaboliczne limfadenopatie obserwowano również u 31 pracowników służby zdrowia po wstrzyknięciu szczepionki Vaxveria opartej na wektorze adenowirusa (13).
Biorąc pod uwagę pacjentów onkologicznych, najbardziej pouczające badanie przeprowadzono na grupie 728 pacjentów, którym podano szczepionkę mRNA BNT162b2 (14). Badanie PET/CT ujawniło hipermetaboliczne węzły chłonne w okolicy pachowej i nadobojczykowej drenujące miejsce wstrzyknięcia szczepionki u 36% osób, które otrzymały pierwszą dawkę i 54% badanych po podaniu drugiej dawki. Hipermetaboliczne węzły chłonne były powiększone u 7% zaszczepionych w pierwszej dawce i u 18% zaszczepionych w drugiej dawce. Obie różnice były istotne statystycznie, wykazując, że wpływ na drenaż węzłów chłonnych był większy po dawce przypominającej, co potwierdza dane z powyższej metaanalizy (12). Jeśli chodzi o związek z zasadniczym nowotworem złośliwym, hipermetaboliczne węzły chłonne uznano za złośliwe u 5% pacjentów, podczas gdy u 15% zaszczepionych, w tym u 16 pacjentów z chłoniakiem, nie można było wyciągnąć żadnych wniosków dotyczących złośliwości. Co ciekawe, w żadnym z tych badań nie rozważano możliwości, że szczepionki mRNA mogły odegrać rolę w rozwoju złośliwych węzłów chłonnych. Rzeczywiście, jak dotąd konsensus jest taki, że występowanie hipermetabolicznych limfadenopatii nie powinno kwestionować bezpieczeństwa szczepionek mRNA ani u osób zdrowych, ani u pacjentów z chorobami nowotworowymi (15).
Według naszej najlepszej wiedzy jest to pierwsza obserwacja sugerująca, że podanie szczepionki SARS-CoV-2 może wywołać progresję AITL. Kilka argumentów przemawia za taką możliwością. Po pierwsze, dramatyczna szybkość i wielkość progresji ujawniła się w dwóch 18F-FDG PET-CT wykonanych w odstępie 22 dni. Taka szybka ewolucja byłaby wysoce nieoczekiwana w naturalnym przebiegu choroby. Ponieważ wiadomo, że szczepienie mRNA indukuje powiększenie i hipermetaboliczną aktywność drenujących węzłów chłonnych, uzasadnione jest przypuszczenie, że to właśnie ono wywołało zaobserwowane zmiany. Rzeczywiście, wzrost wielkości i aktywności metabolicznej był wyższy w pachowych węzłach chłonnych drenujących miejsce wstrzyknięcia szczepionki w porównaniu z ich przeciwległymi odpowiednikami. Jednak istniejące wcześniej węzły chłonne były również wyraźnie wzmocnione w porównaniu z pierwszym testem. Co więcej, nowe zmiany hipermetaboliczne, najprawdopodobniej o charakterze chłoniakowym, pojawiły się wyraźnie w odległości od miejsca wstrzyknięcia.
W rzeczywistości, rzekome wzmagające działanie szczepionki na komórki nowotworowe AITL jest w pełni zgodne z wcześniejszymi obserwacjami identyfikującymi komórki TFH w ośrodkach namnażania jako kluczowe cele szczepionek zawierających zmodyfikowane nukleozydy mRNA, zarówno u zwierząt, jak i u ludzi (1, 2). Złośliwe komórki TFH, jako cecha charakterystyczna AITH, mogą być szczególnie wrażliwe na szczepionki mRNA, gdy zawierają mutację RHOA G17V, która była obecna w omawianym przypadku. Rzeczywiście, ta mutacja ułatwia proliferację i aktywację kilku szlaków sygnałowych w komórkach TFH (16). Co więcej, myszy poddane inżynierii genetycznej w celu reprodukcji mutacji RHOA G17V i TET2 - obydwie były obecne w naszym przypadku - rozwinęły chłoniaka po immunizacji czerwonymi krwinkami owcy (16). Ta eksperymentalna obserwacja jest istotna dla szczepionek RNA, ponieważ wykazano, że RNA czerwonych krwinek owcy jest odpowiedzialne za ich zdolność do stymulowania TFH i wywoływania reakcji ośrodka namnażania (17).
W opisywanym przypadku najpierw pojawia się pytanie, jaką strategię zapobiegania COVID-19 należy zastosować u pacjenta, który jest słabo chroniony przed COVID-19. W perspektywie krótkoterminowej jedyną opcją jest zalecenie ścisłego maskowania i zdystansowania społecznego oraz zaoferowanie mu terapii przeciwciałem przeciwko SARS-CoV-2 w przypadku kontaktu wysokiego ryzyka (16). W dłuższej perspektywie należy wyraźnie unikać stosowania szczepionek mRNA, podczas gdy można rozważyć inne rodzaje szczepionek.
W tej chwili ekstrapolacja wyników omawianego przypadku na innych pacjentów z AITL lub innym chłoniakiem z obwodowych komórek T z udziałem komórek TFH jest przedwczesna. Pacjenci z AITL są rzadcy, a ich profil mutacji jest niejednorodny. Co więcej, ich leczenie może mieć wpływ na ich reakcje immunologiczne. Jest zatem mało prawdopodobne, aby istniejące systemy nadzoru nad bezpieczeństwem farmakoterapii były skuteczne w identyfikowaniu niezwykle rzadkich przypadków, takich jak powyższy. W końcu mogą być potrzebne badania prospektywne obejmujące systematyczne obrazowanie PET/CT po szczepieniu SARS-CoV-2 u pacjentów z AITL z określonymi profilami mutacji. Niezależnie od wyniku takich badań, nie powinien on wpływać na ogólny stosunek korzyści do ryzyka.
Podsumowanie
Omawiana obserwacja, opublikowana jako wstępny wydruk na platformie SSRN (18), sugeruje, że szczepienie szczepionką mRNA BNT162b2 może wywołać szybki postęp chłoniaka angioimmunoblastycznego. Potrzebne są jednak dedykowane badania, aby ustalić, czy ten przypadek można ekstrapolować na populacje pacjentów z AITL lub innym chłoniakiem z obwodowych komórek T z udziałem komórek TFH.
Perspektywa pacjenta
Rzeczony pacjent jest korespondencyjnym autorem opisanego powyżej przypadku, i ma on nadzieję, że niniejszy raport będzie stanowił zachętę do badań mających na celu wyjaśnienie możliwego wpływu szczepienia mRNA przeciwko SARS-CoV-2 na przebieg AITL. Jest również przekonany, że szczepionki mRNA stanowią bardzo wydajne produkty o korzystnym stosunku korzyści do ryzyka.
Oświadczenie o dostępności danych
Oryginalne wkłady przedstawione w niniejszym opracowaniu są zawarte w artykule/materiale uzupełniającym, zaś dalsze zapytania można kierować do autora/ów do korespondencji.
Oświadczenie etyczne
Nie przedstawiono zgody etycznej na przedmiotowe badanie z udziałem ludzi, ponieważ retrospektywna analiza danych PET/CT została zatwierdzona przez Komisję Etyki Hôpital Erasme (ref. P2017/020). Będąc jednym z autorów, pacjent wyraził zgodę na publikację. Pacjenci/uczestnicy wyrazili pisemną świadomą zgodę na udział w tym badaniu. Od osoby (osób) uzyskano pisemną świadomą zgodę na publikację wszelkich potencjalnie identyfikowalnych obrazów lub danych zawartych w tym artykule.
Wkład autorski
Wszyscy wymienieni autorzy wnieśli istotny, bezpośredni i intelektualny wkład w pracę i zatwierdzili ją do publikacji.
Finansowanie
Departament medycyny nuklearnej Hôpital Erasme jest wspierany finansowo przez Fonds Erasme i Association Vinçotte Nuclear (Belgia).
Konflikt interesów
Autorzy deklarują, że badanie zostało przeprowadzone przy braku jakichkolwiek powiązań handlowych lub finansowych, które mogłyby być odebrane jako potencjalny konflikt interesów.
Nota od wydawcy
Wszystkie twierdzenia wyrażone w tym artykule są wyłącznie twierdzeniami autorów i niekoniecznie reprezentują twierdzenia ich stowarzyszonych organizacji lub wydawcy, redaktorów i recenzentów. Żaden produkt, który może być oceniany w tym artykule, lub twierdzenie, które może być wystawione przez jego producenta, nie jest gwarantowane ani popierane przez wydawcę.
Podziękowania
Niniejszy artykuł został opublikowany jako wstępny wydruk na platformie SSRN https://ssrn.com/abstract=3945001. Dziękujemy Alexandre De Wind i Denis Larsimont (Department of Pathology, Jules Bordet Institute, Bruksela, Belgia) oraz Laurence de Leval (Institut Universitaire de Pathologie, CHUV, Lozanna, Szwajcaria) za dodatkowe analizy próbek biopsyjnych oraz Olivier Hermine (Department of Pathology, Necker Hospital, Paryż, Francja) za pożyteczną dyskusję.
Przypisy:
- Pardi N, Hogan MJ, Naradikian MS, Parkhouse K, Cain DW, Jones L, et al.. Modyfikowane nukleozydami szczepionki mRNA indukują silne odpowiedzi komórek B pomocniczych pęcherzyków T i centrum rozmnażania. J Exp Med. (2018) 215:1571. 10.1084/jem.20171450 [darmowy artykuł PMC] [PubMed] [CrossRef] [Google Scholar]
- Turner JS, O'Halloran JA, Kalaidina E, Kim W, Schmitz AJ, Zhou JQ i in.. Szczepionki SARS-CoV-2 mRNA indukują trwałe odpowiedzi ludzkiego centrum rozmnażania. Natura. (2021) 596:109-13. 10.1038/s41586-021-03738-2 [PubMed] [CrossRef] [Google Scholar]
- Özütemiz C, Krystosek LA, Church AL, Chauhan A, Ellermann JM, Domingo-Musibay E, et al.. Limfadenopatia u zaszczepionych COVID-19: dylemat diagnostyczny u pacjentów onkologicznych. Radiologia. (2021) 300: E296-300. 10.1148/radiol.2021210275 [artykuł darmowy PMC] [PubMed] [CrossRef] [Google Scholar]
- Cohen D, Krauthammer SH, Wolf I, Even-Sapir E. Limfadenopatia hipermetaboliczna po podaniu szczepionki BNT162b2 mRNA Covid-19: częstość występowania oceniana za pomocą [18F]FDG PET-CT i znaczenie dla interpretacji badania. Eur J Nucl Med Mol Obrazowanie. (2021) 48:1854-63. 10.1007/s00259-021-05314-2 [bezpłatny artykuł PMC] [PubMed] [CrossRef] [Google Scholar
- Sakata-Yanagimoto M, Enami T, Yoshida K, Shiraishi Y, Ishii R, Miyake Y i in.. Somatyczna mutacja RHOA w angioimmunoblastycznym chłoniaku z komórek T. Nat Genet. (2014) 46:171-5. 10.1038/ng.2872 [PubMed] [CrossRef] [Google Scholar
- Kitadate A, Narita K, Fukumoto K, Terao T, Tsushima T, Kobayashi H i in.. Wyjściowa glikoliza zmian całkowitych w połączeniu z tymczasową pozytronową tomografią komputerową tomografii emisyjnej jest silnym predyktorem rokowania u pacjentów z chłoniakiem obwodowych komórek T. Rak Med. (2020) 9:5509-18. 10.1002/cam4.3226 [artykuł za darmo PMC] [PubMed] [CrossRef] [Google Scholar]
- Horwitz S, O'Connor OA, Pro T B, Illidge, Fanale M, Advani R, et al.. Brentuksymab vedotin z chemioterapią w chłoniaku z obwodowych komórek T CD30-dodatnich (ECHELON-2): globalne, randomizowane badanie III fazy z podwójnie ślepą próbą. Lancet. (2019) 393:229-40. 10.1016/S0140-6736(18)32984-2 [artykuł darmowy PMC] [PubMed] [CrossRef] [Google Scholar]
- Keshavarz P, Yazdanpanah F, Rafiee F, Mizandari M. Limfadenopatia po szczepieniu COVID-19: przegląd wyników obrazowania. Acad Radiol. (2021) 28:1058-71. 10.1016/j.acra.2021.04.007 [artykuł darmowy PMC] [PubMed] [CrossRef] [Google Scholar]
- 9. Weeks J, O'Brien S, Rosenspire K, Dubroff J, Pantel A. rozwijająca się obustronna hipermetaboliczna limfadenopatia pachowa na FDG PET / CT po 2-dawkowym szczepieniu COVID-19. Clin Nucl Med. (2021) 46:1011-2 10.1097/RLU.0000000000003711 [artykuł bezpłatny PMC] [PubMed] [CrossRef] [Google Scholar]
10. Nawwar AA, Searle J, Lyburn ID. Cechy ogólnoustrojowej odpowiedzi immunologicznej po szczepieniu COVID-19 na 18F-FDG PET/CT. Clin Nucl Med. (2021). [Wydanie elektroniczne przed papierowym]. 10.1097/RLU.0000000000003859 [PubMed] [CrossRef] [Google Scholar]
11. Xu G, Lu Y. COVID-19 mRNA limfadenopatia wywołana szczepieniem naśladuje progresję chłoniaka na FDG PET/CT. Clin Nucl Med. (2021) 46:353-4. 10.1097/RLU.0000000000003597 [PubMed] [CrossRef] [Google Scholar]
12. Treglia G, Cuzzocrea M, Giovanella L, Elzi L, Muoio B. Częstość występowania i znaczenie hipermetabolicznych węzłów chłonnych wykrytych za pomocą 2-[(18)F]FDG PET / CT po szczepieniu COVID-19: przegląd systematyczny i meta -analiza. Farmaceutyki. (2021) 14:762. 10.3390/ph14080762 [artykuł darmowy PMC] [PubMed] [CrossRef] [Google Scholar]
13. Shin M, Hyun CY, Choi YH, Choi JY, Lee K-H, Cho YS. Limfadenopatia związana ze szczepieniem COVID-19 w FDG PET/CT: charakterystyczne cechy szczepionki z wektorem adenowirusa. Clin Nucl Med. (2021) 46:814-9. 10.1097/RLU.0000000000003800 [artykuł darmowy PMC] [PubMed] [CrossRef] [Google Scholar]
14. Treglia G, Cuzzocrea M, Muoio B, Elzi L. Wyniki PET po szczepieniu COVID-19: "Keep Calm and Carry On". Obrazowanie Clin Transl. (2021) 9:209-14. 10.1007/s40336-021-00430-3 [darmowy artykuł PMC] [PubMed] [CrossRef] [Google Scholar]
15. Cortes JR, Ambesi-Impiombato A, Couronné L, Bernard OA, Ferrando AA. RHOA G17V indukuje specyfikację komórek pomocniczych pęcherzyka T i promuje limfogenezę. Komórka rakowa. (2018) 33:259-73.e7. 10.1016/j.ccell.2018.01.001 [artykuł darmowy PMC] [PubMed] [CrossRef] [Google Scholar]
16. Loetsch C, Warren J, Laskowski A, Vazquez-Lombardi R, Jandl C, Langley DB i in.. Cytozolowe rozpoznawanie RNA napędza odpowiedź immunologiczną na heterologiczne erytrocyty. Cell Rep. (2017) 21:1624-38. 10.1016/j.celrep.2017.10.044 [PubMed] [CrossRef] [Google Scholar]
17. Cohen MS, Nirula A, Mulligan MJ, Novak RM, Marovich M, Yen C, et al.. Wpływ bamlanivimabu w porównaniu z placebo na częstość występowania COVID-19 wśród mieszkańców i personelu wykwalifikowanej pielęgniarki i placówek opieki: randomizowane badanie kliniczne. JAMA. (2021) 326:46-55. 10.1001/jama.2021.8828 [artykuł darmowy PMC] [PubMed] [CrossRef] [Google Scholar]
18. Goldman S, Bron D, Tousseyn T, Vierasu I, Dewispelaere L, Heimann P i in.. Szybki postęp angioimmunoblastycznych chłoniaków z komórek T po podaniu szczepionki BNT162b2 mRNA Vaccine Booster Shot. Sprawozdanie ze sprawy. Dostępne online pod adresem: https://ssrn.com/abstract=3945001 (dostęp 18 października 2021 r.).
Opracowanie i tłumaczenie: Marek Skowroński